· 式は、 (nh 2) 2 co 4h 2 o → 2nh 3 co 2 2h 2 o → 2nh 4 co 2 2ohで水を加えて分解してアンモニアと二酸化炭素を排出する 分解は水に溶けてから酵素反応という硫安より1ステップ多くなるので、 尿素は硫安の様な速さで肥効を示すことはない ということは尿素は(NH 2) 2 CO の化学式で表される.物性比較を Table1(4)に示す.尿素は熱によりアンモニアに分解 することができるが,ディーゼルエンジンの排気ガ ス後処理システムである尿素SCR システムでは,尿 素の加水分解に180℃以上の高温を要する.そこで, より低エネルギーで尿素をアンモニア尿素(化学式(NH 2 ) 2 CO)を合成する方法。 尿素は動物の尿中に含まれる有機化合物であり、たんぱく質や核酸の分解生成物中の窒素分を体外に排出する役割を受け持っている。 近年、尿素は窒素肥料として、また尿素樹脂などの工業原料として、大量に消費されており、尿素の工業的合成がそれを可能にしている。 一般的な合成法は、アンモニアと炭酸ガスを
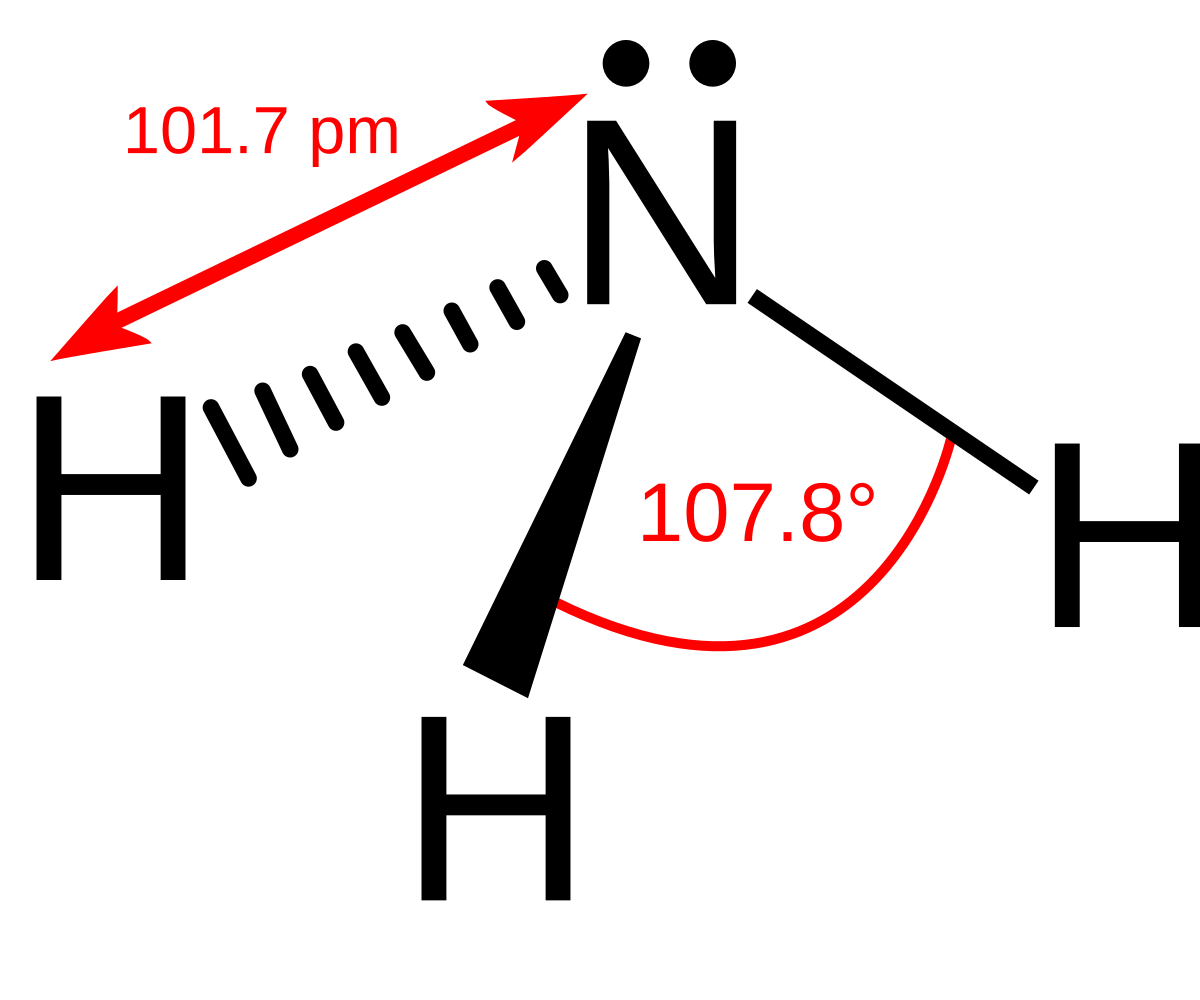
アンモニア Wikipedia
尿素 分解 アンモニア 化学式
尿素 分解 アンモニア 化学式-尿素の加水分解によるアンモニア・炭酸生産の自由エネルギー変化は以下の反応式で表される。 CO(NH 2 ) 2 H 2 O 134 kJ → CO 2 2NH 3 この式は、尿素分解が標準状態では進行しづらく、副生成物であるアンモニアの蓄積が反応を阻 · 尿素を加熱すると。。。 尿素を加熱すると分解してアンモニアなどになってしまうようです。さて、尿素水溶液を加熱した場合、水溶液中で尿素は分解してしまったりするでしょうか?水溶液なので一応100℃以下での場合です。 濃度、水溶液のPH、異物金属イオンの有無等によっても異



中3化学 アンモニアの利用 中学理科 ポイントまとめと整理
Carbamide.CH 4 N 2 O(6005).CO(NH 2) 2 .炭酸のジアミド,カルバミン酸のアミドに相当する.ヒトやほかの動物の体内でタンパク質が分解する際に生成し,尿中に排出される(成人では30 g d -1).植物にもわずかに存在する.クロロギ酸エステル,塩化カルバモイル,炭酸エステル,ホスゲンなどにアンモニアを作用させると生成する.工業的には,液体アンモニアと二酸化成分含有量 浸透圧 アンモニア 0.50気圧 : 21.2% 溶解度曲線図 > 2) 硝酸アンモニウム(硝安) Ammonium nitrate 化学式 NH4NO3 = 80.04使用され 現在アンモニアの製造方法としては,ドイツ人のハーバーとボッシュが1913年に実用化した鉄 触媒を用い水素と窒素からの合成方法が現在でも使用されており,三菱重工エンジニアリン 尿素の加水分解によるアンモニア・炭酸生産の自由エネルギー変化は以下の反応式で表される。 CO(NH 2 ) 2 H 2 O 134 kJ → CO 2 2NH 3 この式は、尿素分解が標準状態では進行
· 尿素は化学式 (nh2)2co 。 無色の結晶 尿酸はプリン体が代謝分解されて出来る最終産物。 化学式c5h4n4o3。 尿素は尿酸がさらに代謝をうけてアンモニア(nh3)となり、二酸化炭素(co2)と反応して排泄される物。 つまり、体内の尿素は尿酸から変換されたもの。 · アンモニア(NH 3 )にプロトン(H )が付加することで生成される。従来のアンモニア直接分解(式1)は吸熱反応である。 そのため、装置の起動時に触媒層を常温から400℃以上 に加熱する必要があり、スイッチオンしてから水素生成ま でに時間と外部加熱を要するという問題がある。また、同 様の理由によって、反応中に常に触媒を外部から加熱する 必要が
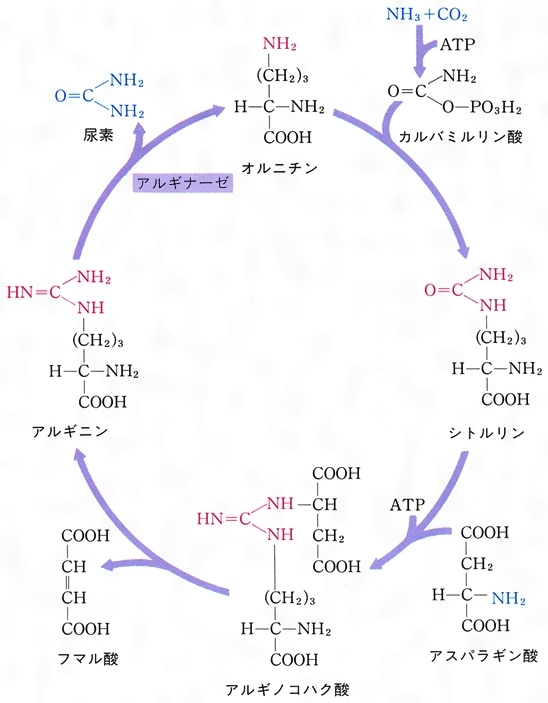
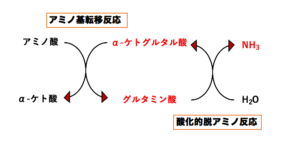
→タンパク分解酵素が作用して 個々のアミノ酸に分解される。 短鎖カルボン酸 (=有機酸) アミノ酸の分解過程では まずアミノ基がはずされ アンモニアが発生する。 尿素サイクルの全体像 オルニチン アルギニン アルギニノ コハク酸 カルバミル リン酸 アンモニア +重炭酸 シトルリン42 IHI 技報 Vol54 No1 ( 14 ) 移動体のディーゼル車の場合は,第2 図に示す尿素水 を分解して生成するアンモニアを用いるSCR 装置 ( 9 ) が 04 年ごろから搭載されている.ディーゼル車用のアン化学名 : 尿素 成分及び含有量 : 尿素99.0%以上 化学式又は構造式 : (NH2)2CO 分子量(式量) : 60.06 官報公示整理番号 : 化審法2-1732 CAS No. : 57-13-6 3.危険有害性の要約
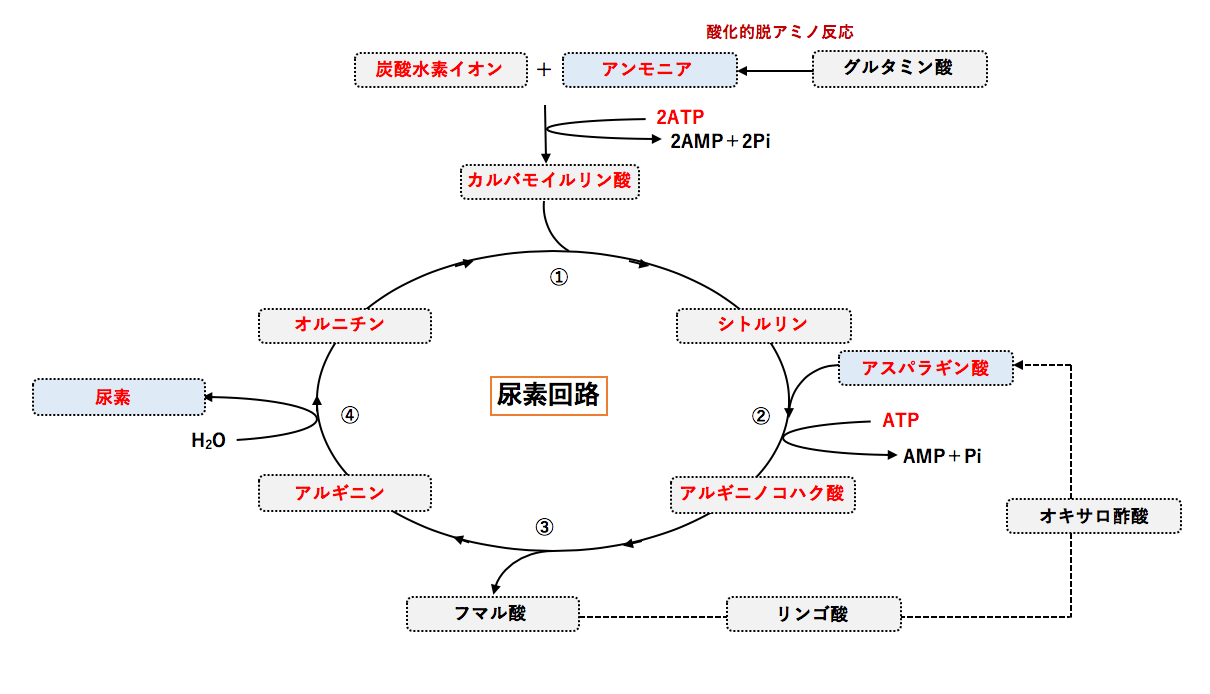



解決 尿素回路の反応と酵素について




施肥について整理 アクアリウム Life
排気ガスを分解する尿素水溶液 日産化学工業 AdBlue アドブルー L 尿素 化学式:CH4N2O 化学名:尿素 CAS No: 化審法化学物質:(2)1732 内容量:L ※濃度48%品を基本に、水酸化ナトリウム濃度範囲~32%品を取り揃え、販売しております。 物性・外観 物理的状態:液体尿素水 (NH2)2CO H2O 排気ガス NOx (100℃~700℃) 尿素の加熱分解(133℃以上) (NH2)2CO →HNCO NH3 イソシアン酸の加水分解(350℃以上)別名 : 尿素水 化学特性(化学式等) : (nh2)2co h2o 成分及び濃度又は濃度範囲(含有量) : ~40% 60~80% (尿素水) : 318~333% 667~6%(アドブルー,スターブルー) 官報公示整理番号(化審法・安衛法) : (2)1732 該当しない cas番号 : 4




アンモニアを含んだ排水の処理 水処理に関するご相談は 栗田工業
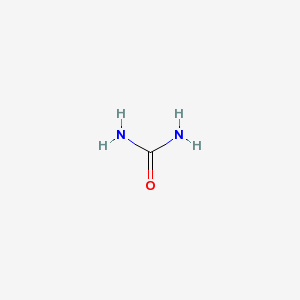



尿素とは何 Weblio辞書
告されている(1).これは,例えば下記の反応式に示す尿素分解 反応により生成するアンモニアがnox 浄化反応の還元剤とし て働くが,この時のアンモニア生成効率が尿素水の拡散状態 に左右されることに起因する. 尿素加水分解反応: (nh2)2co h2o → 2nh3 co24) 有機化合物である尿素は、土壌中にほどこされると水溶液としてそのまま、あるいは微生物的作用や 化学的作用によってアンモニア態窒素(炭酸アンモニウム)に分解(無機化)され、植物に吸収されます。 n = 窒素 o = 酸素 c = 炭素 h = 水素尿素(H 2 NCONH 2 )をアンモニア(NH 2 )と二酸化炭素(CO 2 )に加水分解する反応(H 2 NCONH 2 +H 2 O→2NH 2 +CO 2 )を触媒する酵素。 国際生化学連合(現在は国際生化学・分子生物学連合)の酵素委員会が制定した酵素番号はEC3515。系統名はウレアアミドヒドロラーゼUrea amidohydrolase。




13 号 尿素の電気分解による選択的触媒還元 Astamuse




13 号 尿素の電気分解による選択的触媒還元 Astamuse
尿素は,アンモニアを高温・高圧下で二酸化炭素と反応させて合成するということ。 反応式は必ず書けるようにしてください。 ③のポイントは 尿素樹脂は,尿素とホルムアルデヒドから合成され, 尿素樹脂(尿素のことを英語でureaというのでユリア樹脂とも尿素の分解反応は次の2式で表される。 (NH 2 ) 2 CO=HNCO+NH 3 ・・・① 尿素 イソシアン酸 アンモニア化学名 アンモニア水(水酸化アンモニウム) 化学式 NH 4 OH 英語名 ammonia solution, ammonia water, ammonium hydroxide アンモニア水の特徴 アンモニアガスの水溶液で、薬局で市販されているものは10%溶液です。比較的手軽に入手できます。 やや強いアルカリ性を
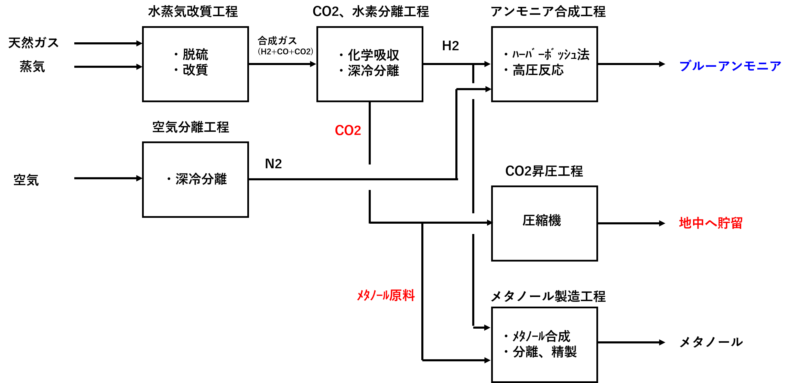



ブルーアンモニアは実用化済み プラントエンジニアがブルーアンモニア グリーンアンモニアを解説



尿素回路
アンモニア(化学式 NH 3)を合成する方法。 実験室では、塩化アンモニウム NH 4 Clを消石灰 Ca(OH) 2 と熱して生成する。 2NH 4 Cl + Ca(OH) 2 → 2NH 3 + CaCl 2 + 2H 2 O 工業的には、石炭の乾留で生成する石炭ガスを水で洗浄した時に生じるガス液に石灰を加えて蒸留し、そこに含まれているアンモニア尿素分解・嫌気的アンモニア酸化反応共役で拓く「高速」「高 尿素の加水分解によるアンモニア・炭酸生産の自由エネルギー変化は以下の反応式で表される。 co(nh2)2 h2o 134 kj → co2 2nh3 この式は、尿素分解が標準状態では進行しづらく、副生成物であるアンモニアの蓄積が反応を阻 アンモニアの化学式塩基性物質として出題される。 今回は、アンモニアの化学式(1)式で用いる二酸化炭素CO 2 は,石灰石CaCO 3 を熱分解してつくる。 このとき同時に生じる酸化カルシウムCaOは,水と反応させて水酸化カルシウムCa(OH) 2 としたのち,(1)式の反応で生じる塩化アンモニウムNH 4 Clと混合して熱し,アンモニアを回収する。



3 自然界における窒素の循環 農業における窒素循環の視角から循環型社会を展望する 大串 和紀 Seneca 21st




第2節 肝臓と腎臓の働き
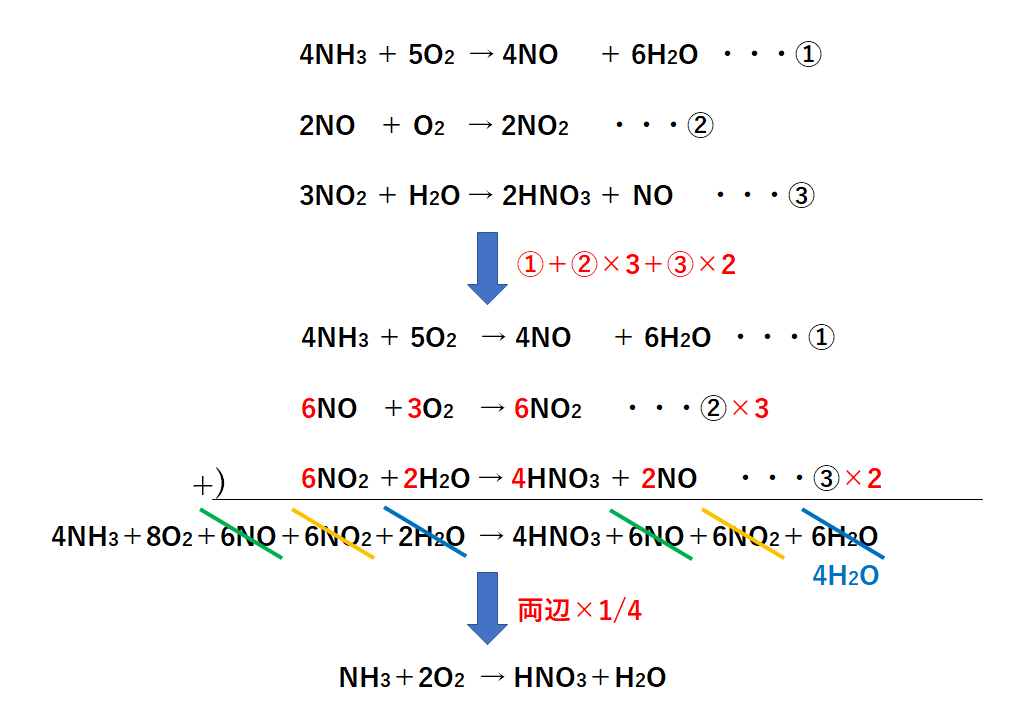
尿素回路の全体の反応((1)~(5))は次のようになる。2 nh 3 co 2 3 atp 2 h 2 o → nh 2 conh 2 2 adp 2 p i amp pp i 図から分かるように、尿素の2つのnh 2 基のうち、1つはアンモニア由来、もう1つはアスパラギン酸由来である。 また、カルボニル基は段階(1)で結合した二酸化炭素(正しくはhco 3)に反応式は、 (nh 2) 2 co 2h 2 o → (nh 4) 2 co 3 アンモニアが通気性の良い環境に於いて土壌微生物によりさらに亜硝酸を経由して硝酸 に酸化される。この過程は硝化作用(硝酸化成)と呼ばれる。反応式は、 2nh 4 3o 2 → 2no 2- 2h 2 o 4h 2no 2- o 2 → 2no 3- 尿素はそのままの形では植 · アンモニアと炭酸ガスを原料とした尿素合成の機構は 次の2式 に示すごとき逐次反応であり,温度に応じた圧 力をかけて適当な反応時間を与える通 常,圧 力150~ 250atm,温 度180~0℃ の反応条件が用いられる 2NH3(l)CO2(g) NH4CO2NH2(l) (1) アンモニウムカーバメー ト**




第2節 生物のつくる物質



話0001
れる。本装置では、尿素分解触媒を用いて②式 の反応を促進することで、反応器内で尿素をア ンモニアにほぼ100%分解することができる。 また、発生したアンモニアは、輸送ブロワによ 株式会社タクマ エンジニアリング統轄本部 技術センター 技術開発部 〒 兵庫県尼崎市金楽寺町2233 · 「 アンモニア(NH3 )」が発生します。 CO(NH2)2 H2O → CO2 2NH3 ↑化学式 :生物の排泄物である「尿素CO(NH 2 ) 2 」が分解されて「アンモニアNH 3 」になります。




アドブルー Nox還元添加剤 事業 製品 三井化学株式会社



特許 知財ポータル Ip Force
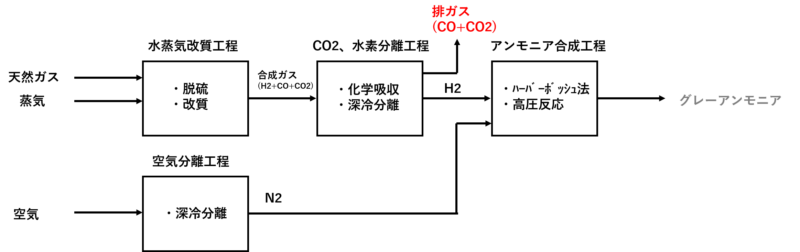



ブルーアンモニアは実用化済み プラントエンジニアがブルーアンモニア グリーンアンモニアを解説



製品情報 脱硝用 尿素水 概要 フォレコ株式会社




アンモニア Wikipedia
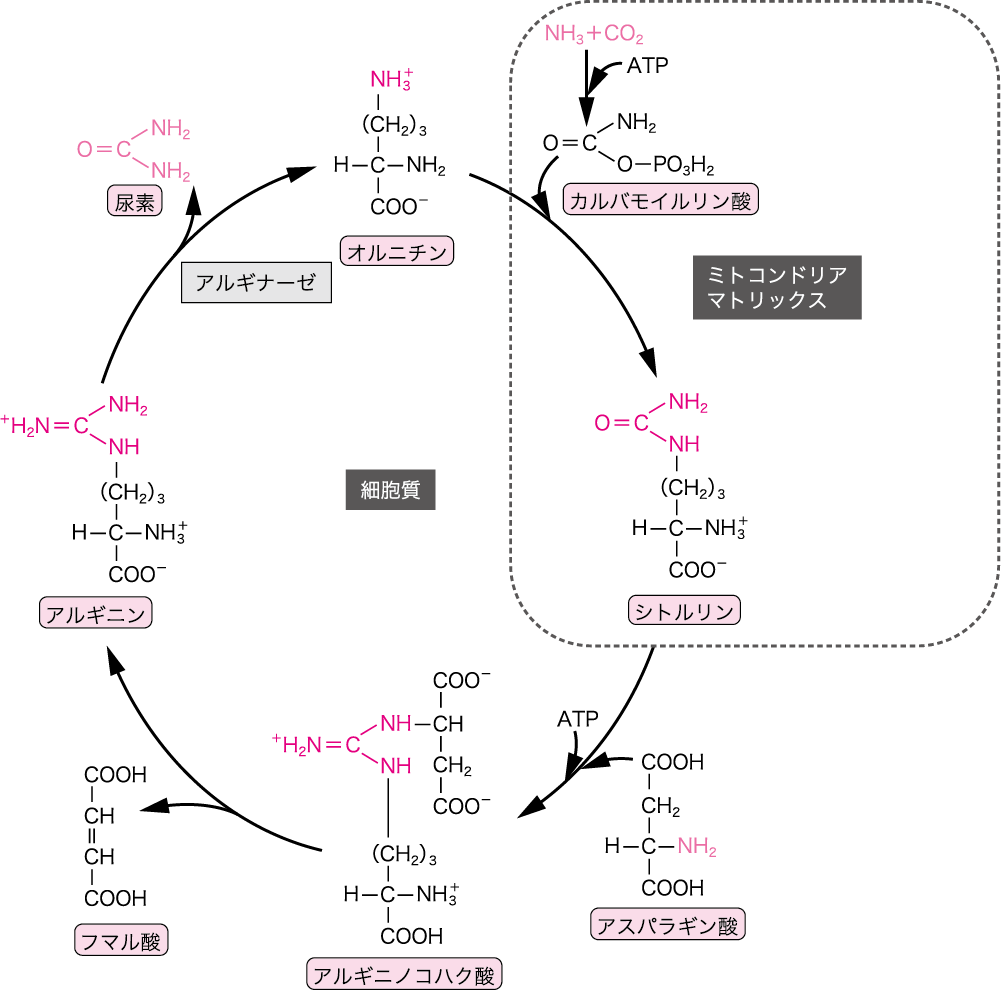



6 尿素回路 Urea Cycle ニュートリー株式会社




Jpb2 尿素を出発物質で使用するヒドラゾジカルボンアミドの製造方法及び装置 Google Patents




05 27号 尿素水を用いる排ガス脱硝装置 Astamuse
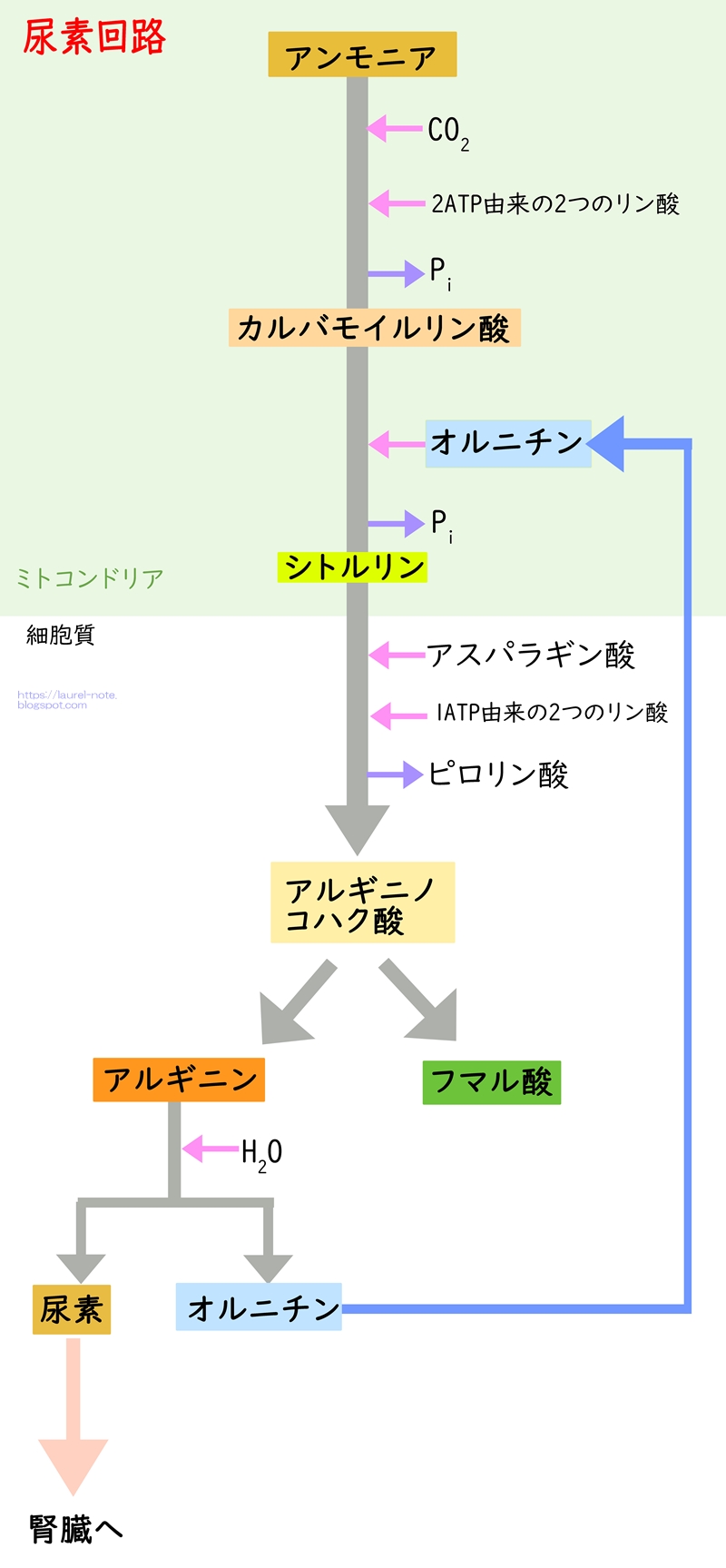



キャラ化 尿素回路 オルニチン回路 をわかりやすく解説



クレアチンとクレアチンリン酸



脱硝システム用尿素水分解解析プログラム
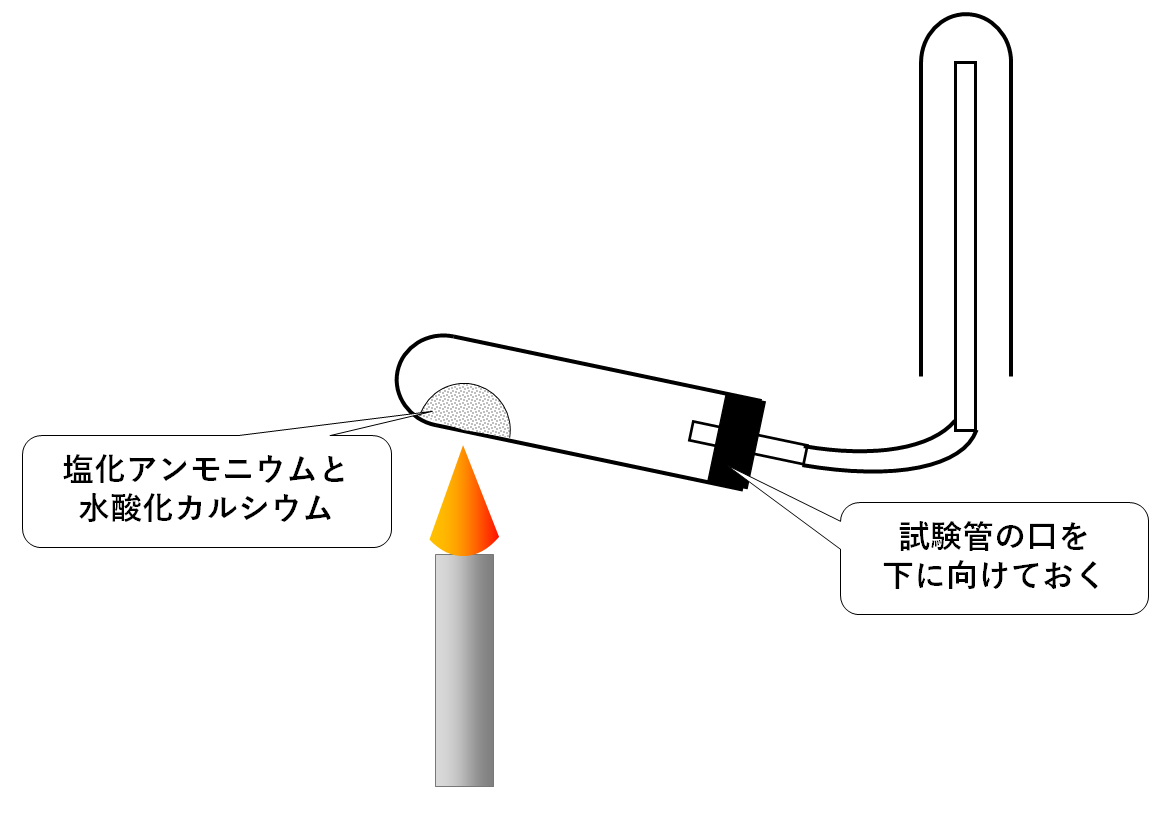



中3化学 アンモニアの利用 中学理科 ポイントまとめと整理
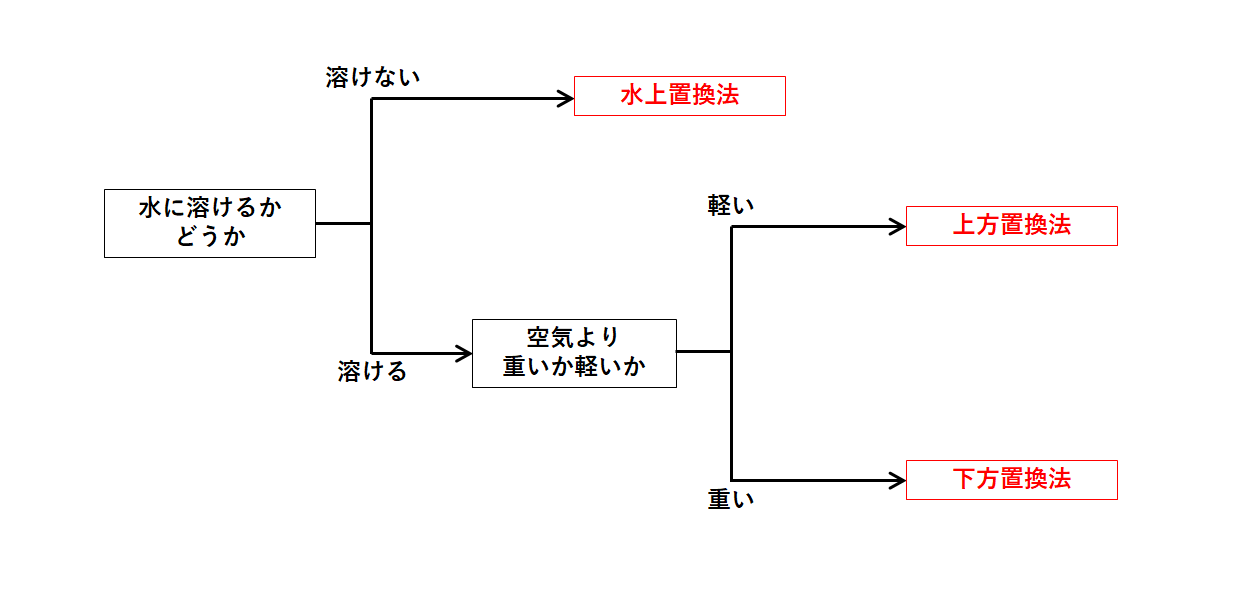



気体の性質まとめ 中学理科 ポイントまとめと整理



実験13 アンモニアの噴水 1年理科 化学 Takaの授業記録12




尿素が少ない になるのはなぜですか 開設お願いします Clear
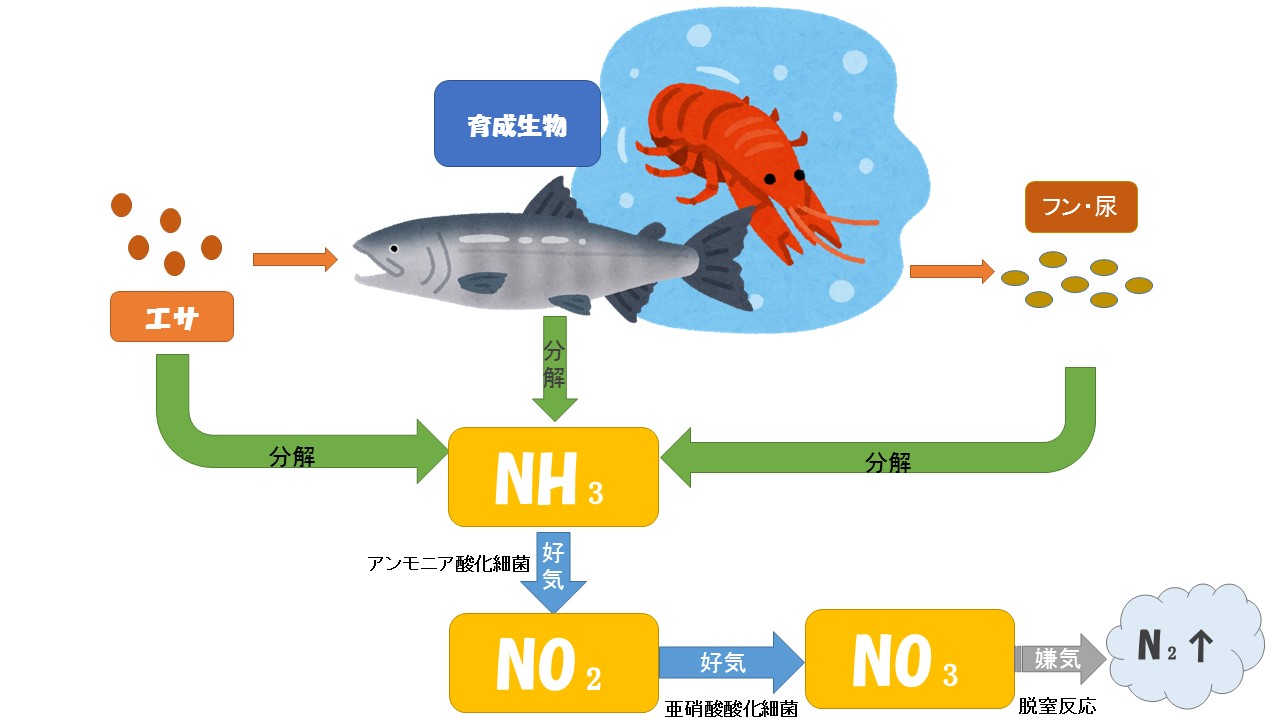



水質管理 窒素循環について アンモニア 亜硝酸 硝酸 持続可能な農業 養殖ビジネス




美しい 化学式 アンモニア Minecraftの最高のアイデア



尿素回路
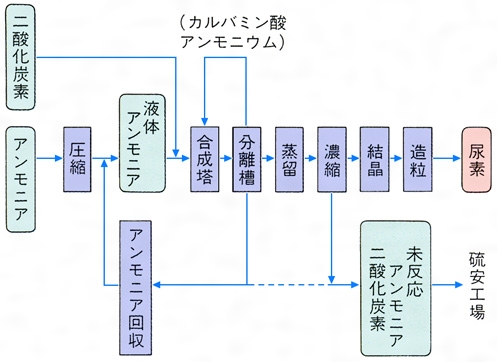



尿素とは コトバンク




第2節 肝臓と腎臓の働き
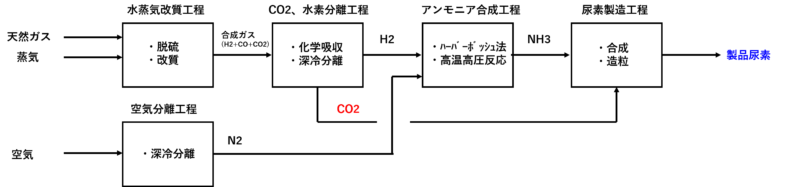



ブルーアンモニアは実用化済み プラントエンジニアがブルーアンモニア グリーンアンモニアを解説



日本肥料アンモニア協会
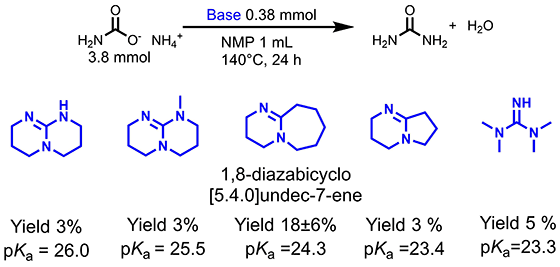



廃水中のアンモニアを資源に変える触媒を発見 有害物質処理から有用物質製造へ 東工大ニュース 東京工業大学




化学工業の歴史1 無機 有機化学工業の基盤成立 化学工業の基礎知識2 ものづくり まちづくり Btob情報サイト Tech Note



尿素回路
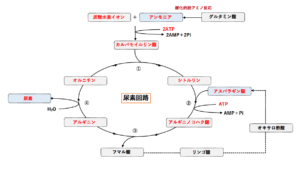



解決 尿素回路の反応と酵素について
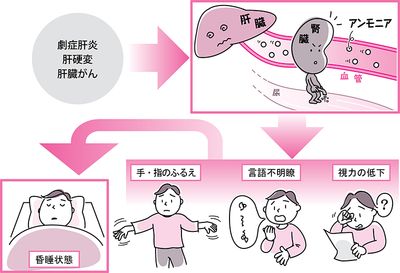



アンモニアとは コトバンク



アミノ酸の分解



尿素 化学式 尿素は硫安の様な速さで効くか



特許 知財ポータル Ip Force



特許 知財ポータル Ip Force



icho34 2002



オルニチン回路とは コトバンク




尿素 化学式 尿素は硫安の様な速さで効くか



滅菌された尿素水溶液およびその製造方法




尿素scrシステムについて アドブルーと同等品質の尿素水なら低価格のオプティ エコツーライト



中3化学 アンモニアの利用 中学理科 ポイントまとめと整理



アンモニアが 燃料 になる 前編 身近だけど実は知らないアンモニアの利用先 スペシャルコンテンツ 資源エネルギー庁



解決 グルタミン酸とグルタミンを介したアンモニアの体内輸送




ブルーアンモニアは実用化済み プラントエンジニアがブルーアンモニア グリーンアンモニアを解説




尿素 Wikipedia




13 号 尿素の電気分解による選択的触媒還元 Astamuse




化学関係単語カード Quizlet
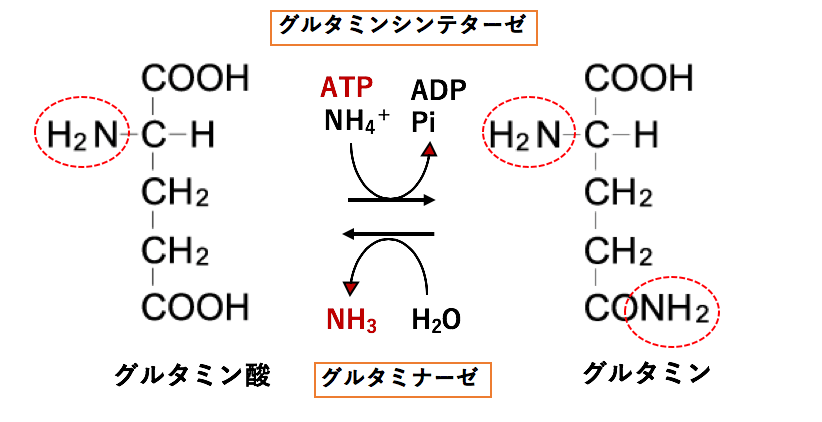



解決 グルタミン酸とグルタミンを介したアンモニアの体内輸送




この図で 尿素が1番少ない血液が流れている i Clear




尿素回路 Wikipedia




尿素 Wikipedia
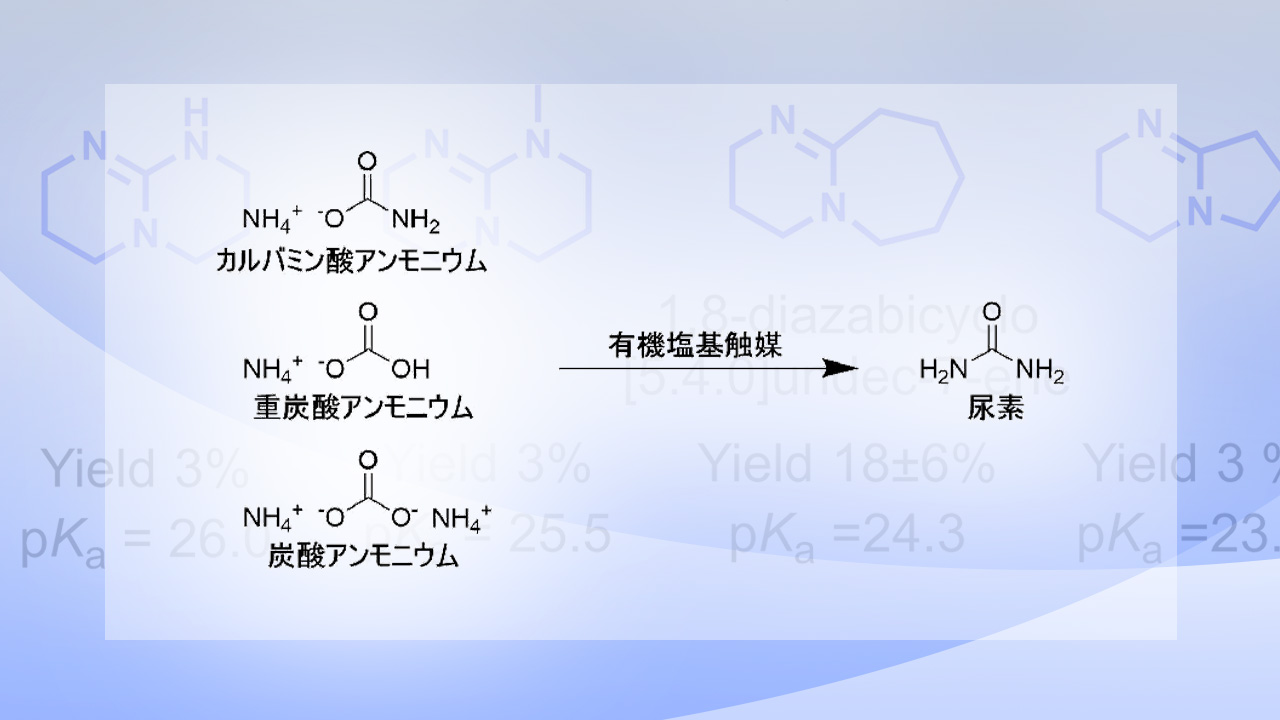



廃水中のアンモニアを資源に変える触媒を発見 有害物質処理から有用物質製造へ 東工大ニュース 東京工業大学
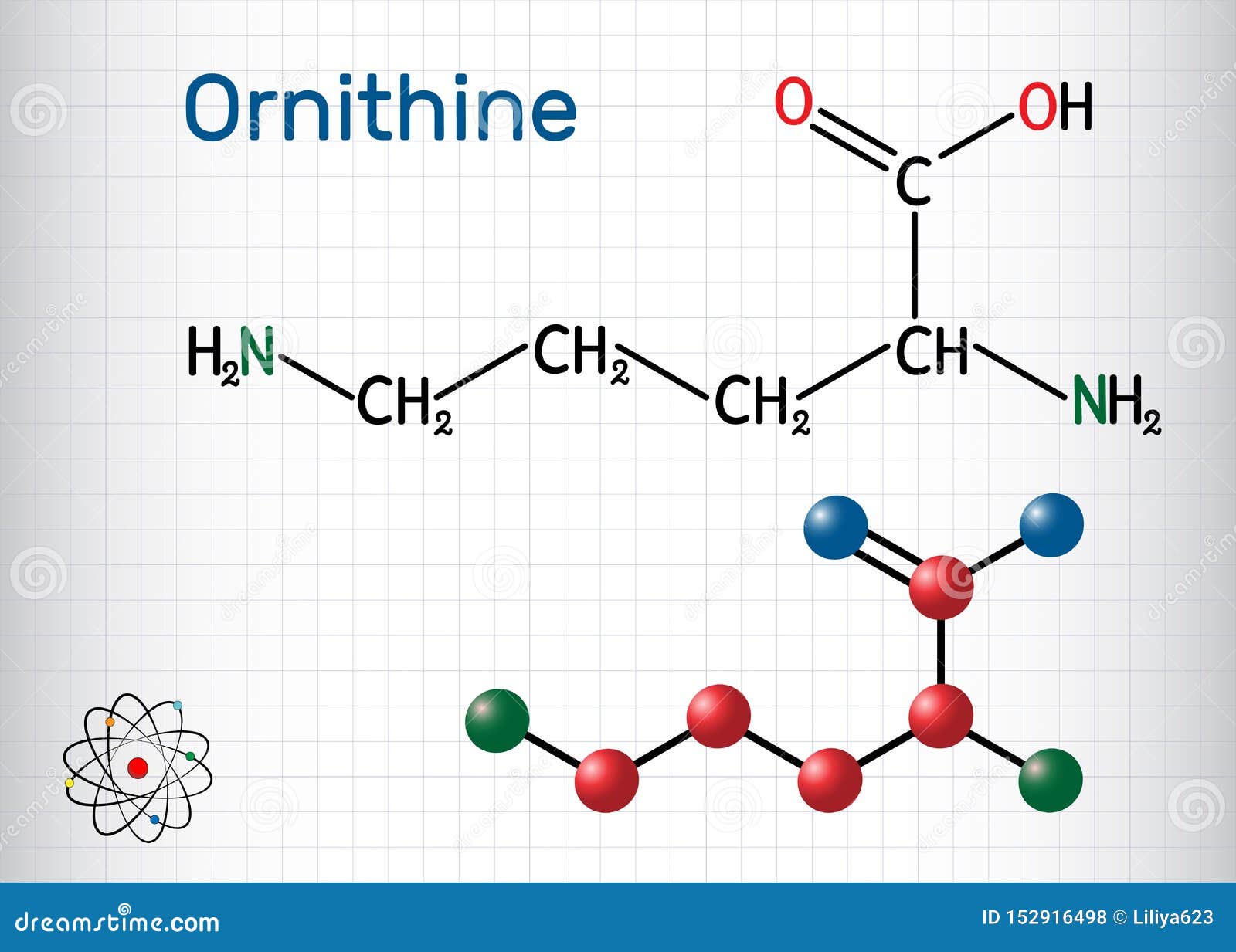



尿素 化学式 尿素は硫安の様な速さで効くか



観賞魚の水質管理について 環境浄化および微生物の応用
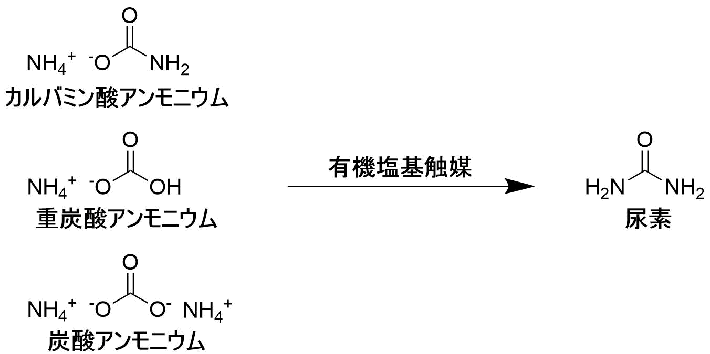



廃水中のアンモニアを資源に変える触媒を発見 有害物質処理から有用物質製造へ 東工大ニュース 東京工業大学



日本肥料アンモニア協会
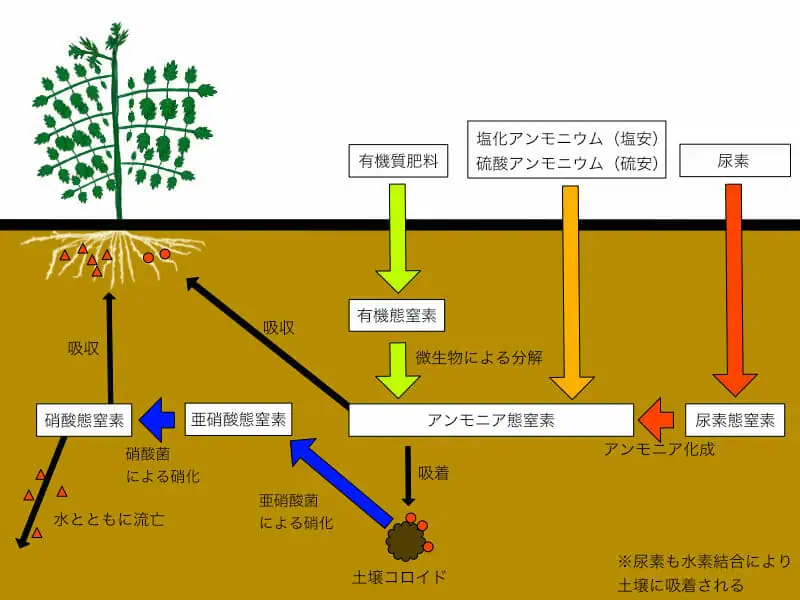



植物の生長に絶対に必要な要素 窒素質肥料の基本 農家web
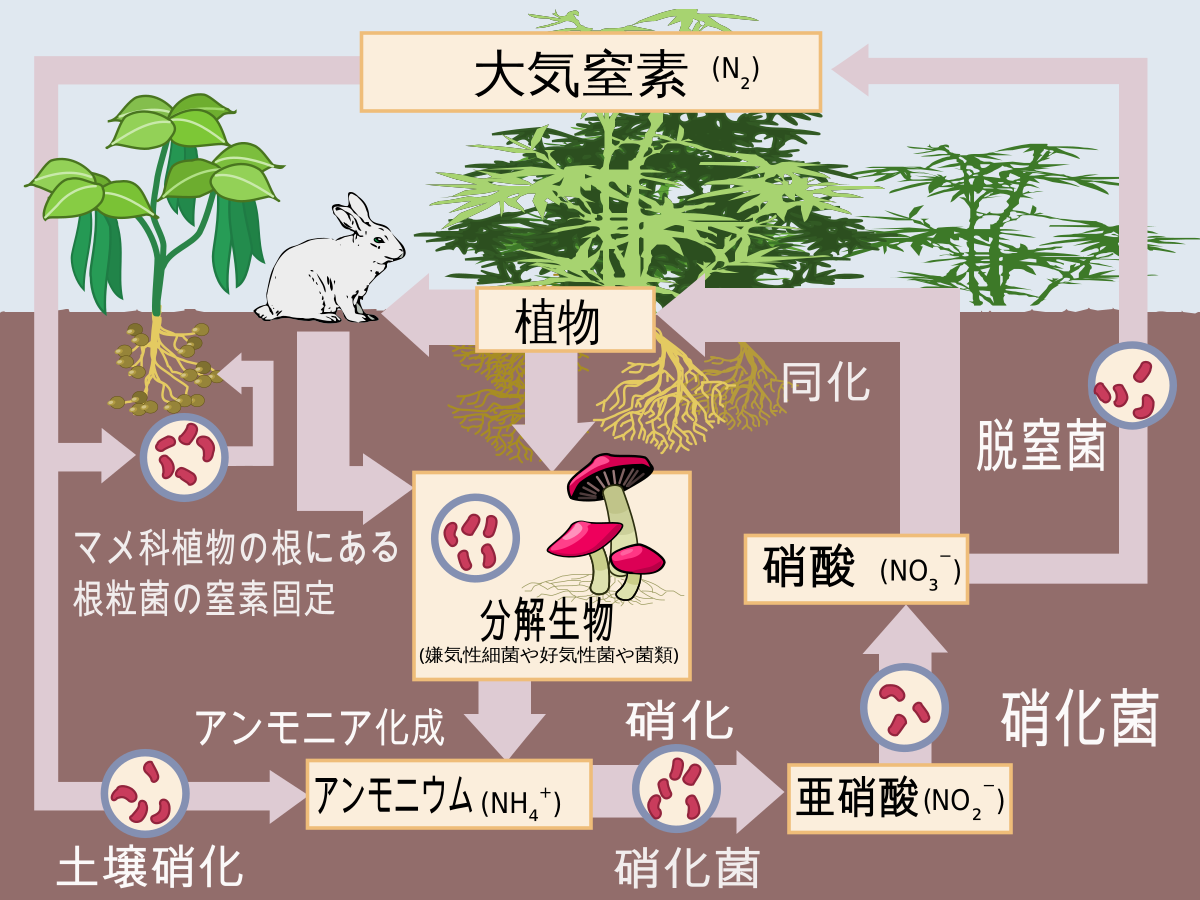



硝化作用 Wikipedia



6 11月13日 オルニチン回路
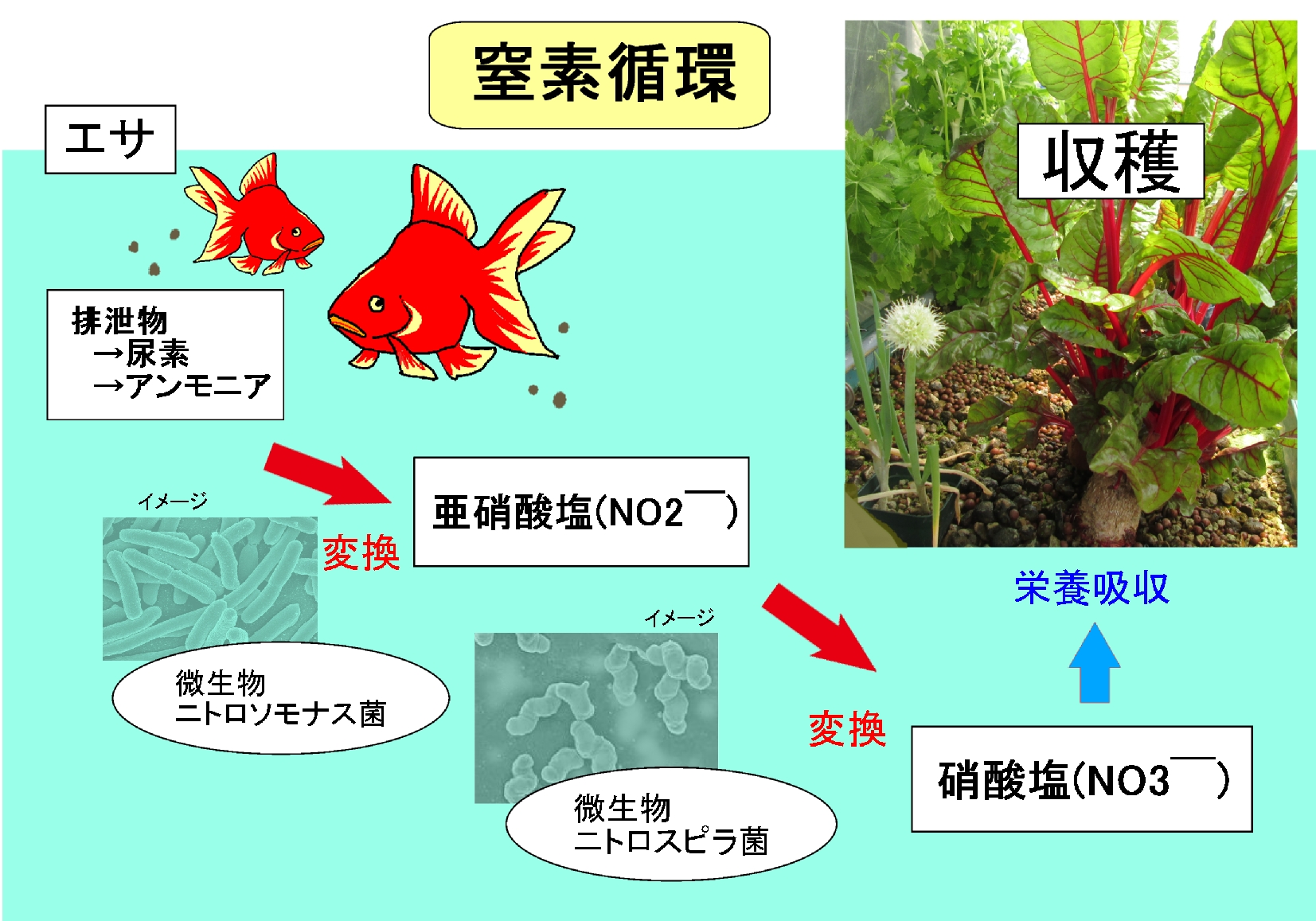



魚のフンが栄養になる仕組み ぼんちすとのアクアポニックス




以外の問題を教えてください お願いします Clear
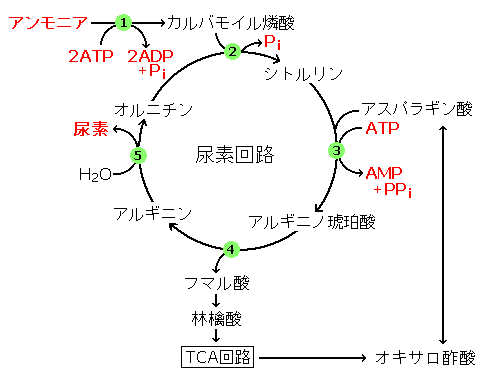



尿素回路 通信用語の基礎知識



マメ知識 水草水槽の微生物 その アクアフォレスト
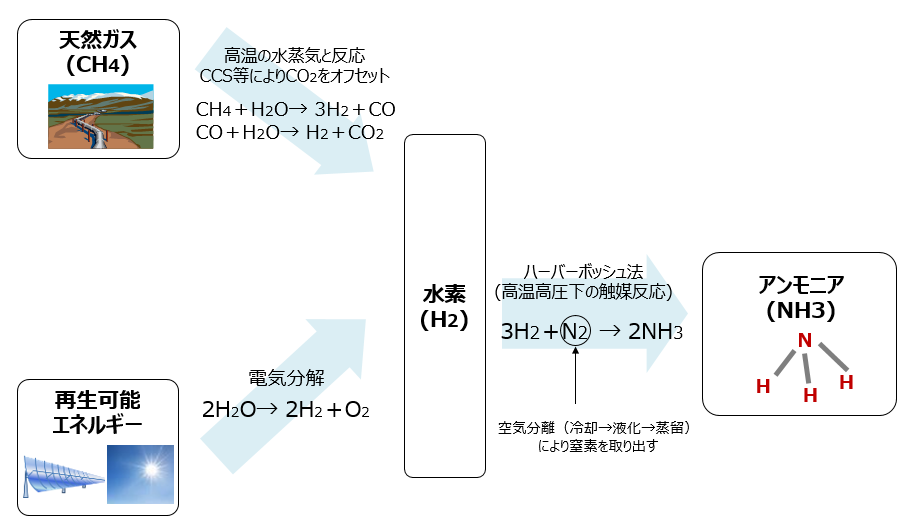



アンモニアが 燃料 になる 前編 身近だけど実は知らないアンモニアの利用先 スペシャルコンテンツ 資源エネルギー庁



新日本化成株式会社 Adblue のご案内



Tnueivp37bifnm
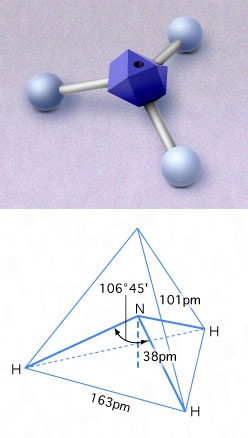



アンモニアとは コトバンク



炭酸アンモニウム Wikipedia




第2節 生物のつくる物質
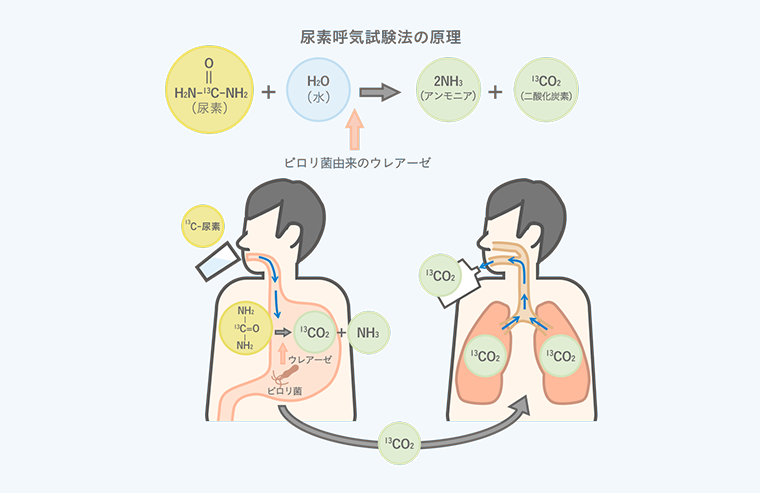



ピロリ菌の検査と除菌治療 大塚製薬
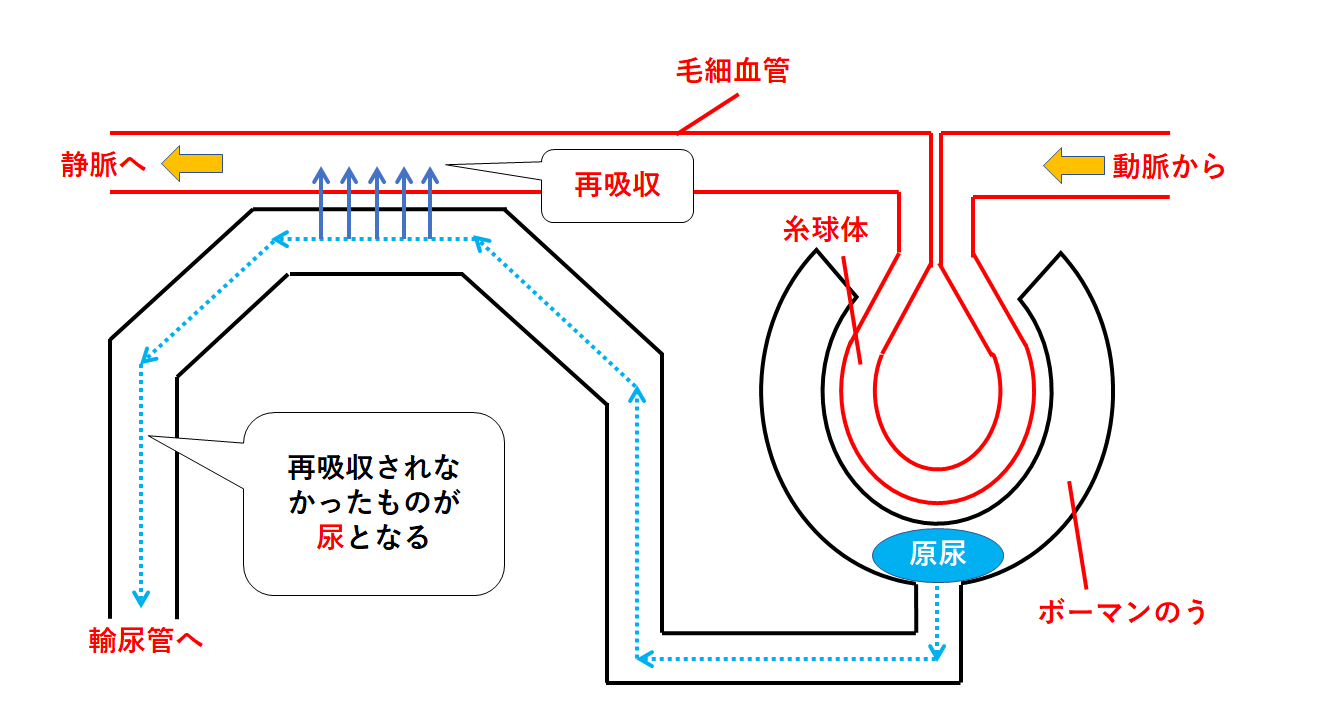



中2生物 腎臓 排出のしくみ 中学理科 ポイントまとめと整理




尿素 化学式 尿素は硫安の様な速さで効くか



尿素 化学式 尿素は硫安の様な速さで効くか



生化学 尿素回路 だーもものblog




中3化学 アンモニアの利用 中学理科 ポイントまとめと整理




5 3 2 肥料




微生物の働きで窒素化合物を除去する生物脱窒法 水処理に関するご相談は 栗田工業




有機化合物100選ボット No Twitter 86 尿素 常温常圧で無色の結晶 保湿剤 肥料 樹脂の原料に用いられる 生化学実験では生体高分子の変性剤として用いられる 人体がとりいれた窒素は尿素 として排泄される 尿素回路 工業合成 アンモニア 二酸化炭素 尿素




第2節 生物のつくる物質




13 号 尿素の電気分解による選択的触媒還元 Astamuse



尿素 Wikipedia
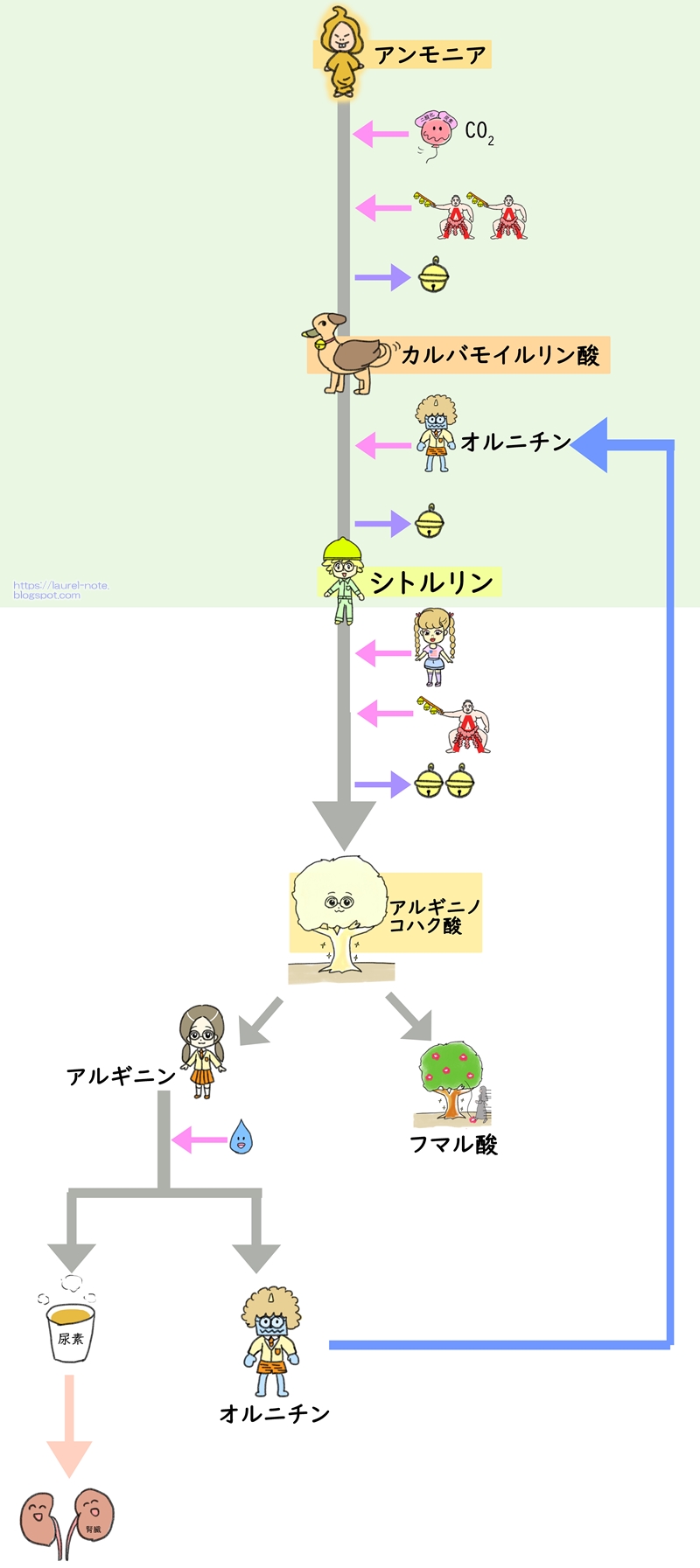



キャラ化 尿素回路 オルニチン回路 をわかりやすく解説




キャラ化 尿素回路 オルニチン回路 をわかりやすく解説




オルニチン回路 脱仙人からの昇天 からのぶろぐ
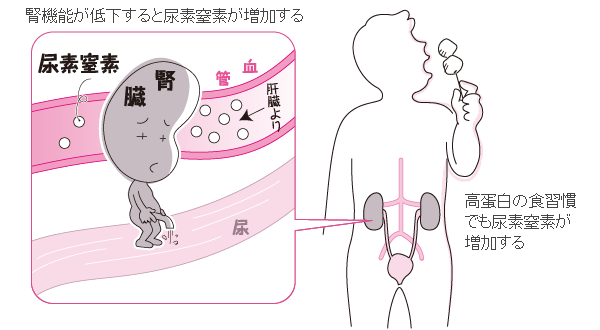



尿素窒素とは 病気の検査法を調べる 医療総合qlife


